研究内容
有機合成化学は、化学反応を自在に操ることで、目的とする分子を精密に組み立てることができる、非常に魅力的な分野です。この分子構築技術は、医薬品の創製にとどまらず、医薬品を疾患部位に届けるドラッグデリバリーや、様々な治療に利用できる生体材料といった幅広い分野を支える基盤となっており、基礎から応用まで多様な研究領域へとつながっています。
当研究室では、「欲しい分子を自在に作れる」という有機合成化学の本質的な魅力を最大限に引き出すことを目指しています。つまり、このような分子構築を効率的かつ選択的に達成できる独自の反応や触媒の開発に取り組んでいます。さらに、これらの基盤技術を活かし、ペプチドやタンパク質といった生体分子の精密な構造変換へと展開することで、創薬やドラッグデリバリー、生体材料開発に貢献する新しい分子変換技術の創出を目指していきます。さらに、製薬企業での工業化研究の経験も活かして、実際に医薬品工業において便利に利用できるような実践的な方法論や試薬へと磨き上げていくことも目指します。有機合成を基盤に、生命科学や医薬分野へと広がる研究に挑戦したい学生を歓迎します。
ジスルフィドのモジュラー合成を可能にする試薬開発
硫黄原子が2つ連結したジスルフィドは、様々な生物活性天然物に含まれるのみならず、生体内で切り離し可能なリンカーとしてのドラッグデリバリーにおける利用や、ペプチド創薬、酸化還元特性を利用した材料開発などにおいて重要な構造です。一方で、両側に異なる置換基を有する非対称ジスルフィドの構築は困難でした。

当研究室では最近、ジスルフィド上に、使い分けて変換可能な2つの脱離基を有する新たなモジュラー型ジスルフィド試薬の開発に成功しています。本試薬は、酸性条件では優先的なプロトン化を経てアミノ基側が、中性・塩基性条件では本質的に電子不足なイミド基側で変換を行うことができ、これらの変換を組み合わせることで、多彩な構造有する非対称ジスルフィドを、短段階で合成可能です。本試薬は、非常に安定で取り扱いやすい固体であり、優れた反応性を示すため、現在試薬メーカーでの発売に向けて検討中です。
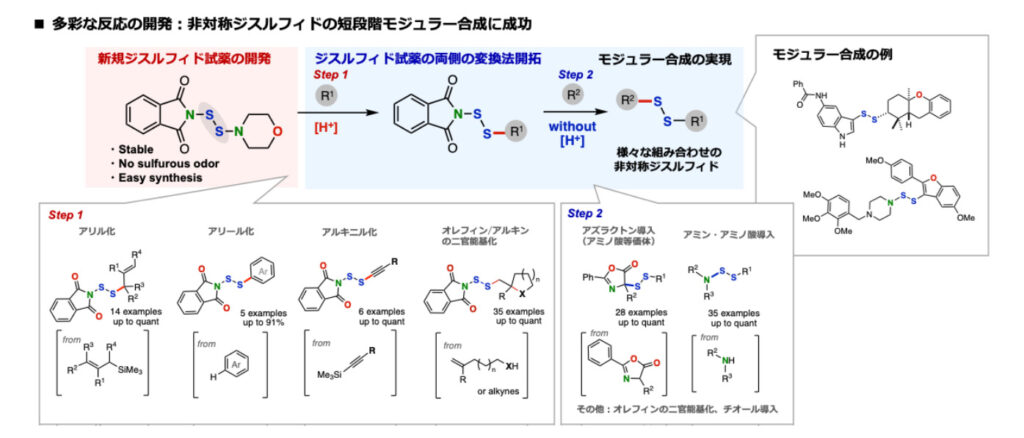
本試薬は、両側で多彩な変換に用いることができ、最近では多彩なヘテロ環の構築や、オリゴペプチドへのジスルフィド導入、複数の機能を併せ持ったジスルフィドなど多岐にわたるジスルフィドの合成に成功しています。
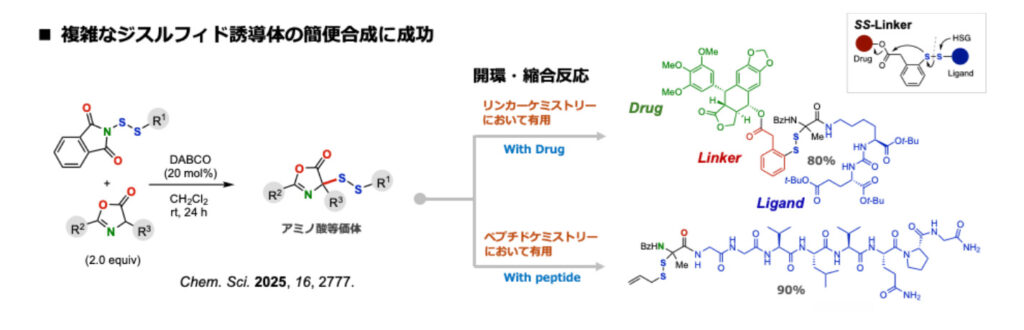
現在は、より高活性な試薬、立体選択的な反応が可能な試薬、求電子的な変換から更に反応性を拡張できる試薬、硫黄数の多いポリスルフィド合成に利用できる試薬など、新たな試薬の開発に取り組んでいます。また、生体内の還元的な環境で切り離し可能なジスルフィドの特性を利用した、ドラッグデリバリーのリンカー構造としての展開にも取り組んでいく予定です。
<関連の業績>
Angew. Chem., Int. Ed. 2023, 62, e202219156.
Org. Chem. Front. 2026, 13, 1299.
J. Org. Chem. 2026, 91, 1817.
Chem. Sci. 2025, 16, 2777.
Org. Lett.2024, 26, 438.
ペプチドのピンポイント修飾法の開発

ペプチドはタンパク質を構成する基本単位であり、生命現象の制御に深く関与するとともに、生体材料としても大きな可能性を秘めています。一方で、ペプチドは多様な求核性部位を有するため、狙った位置のみを選択的に変換することは依然として容易ではありません。本研究室では、この課題を解決するための新たな分子変換手法の開発に取り組んでいます。
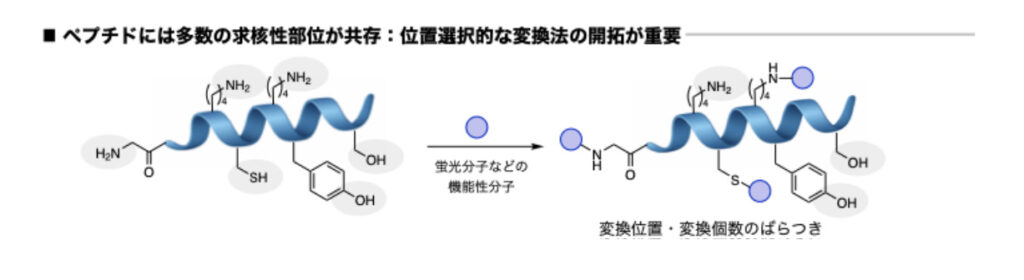
最近私たちは、多くの場合1か所しか存在しないN末端のみで選択的に分子連結を行う新たな方法論を開発しました。本手法により、N末端に対して二つの機能性分子を一挙に導入することが可能となります。また、長鎖のペプチドであっても非常に効率よく進行します。加えて、セリンやシステインなど様々なアミノ酸残基から選択的に発生可能なデヒドロアラニンを用いることで、二種のペプチドを精密に連結する技術の確立にも成功しました。
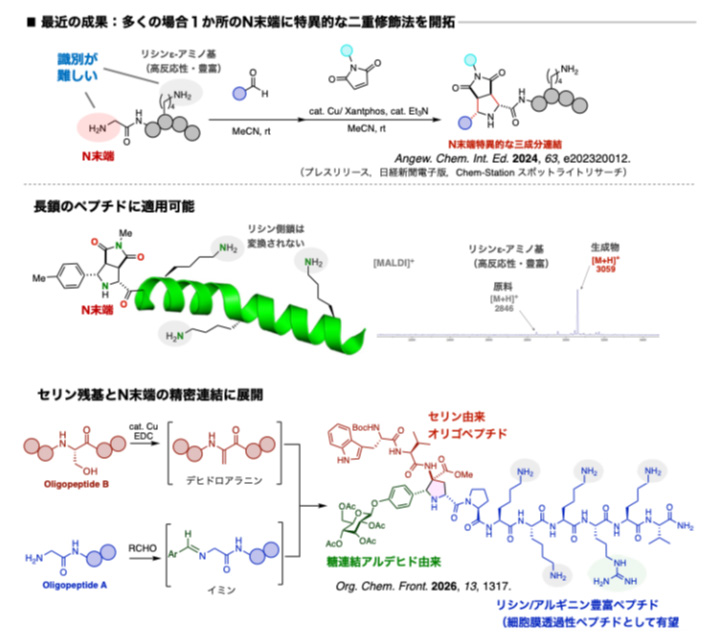
現在は、N末端にとらわれない新たなピンポイントペプチド連結反応の開発に取り組んでいます。また、タンパク質の機能改変のような高度な応用研究にも取り組んでいます。加えて、2成分の機能性ペプチドを簡便に集積できる特徴を活かした、多機能性材料の開発にも取り組んでいます。
<関連の業績>
Angew. Chem., Int. Ed. 2024, 63, e202320012.
Org. Chem. Front. 2026, 13, 1317.
立体選択的な反応の開発と創薬基盤構築への展開
アミノ酸にはキラリティが存在し、生命現象における分子認識に重要な役割を果たしています。また、アミノ酸の連結体であるペプチドやタンパク質にも多数の不斉点が含まれています。当研究室では、アゾメチンイリドを基盤とした非天然アミノ酸の不斉合成に加え、ペプチドを対象とした不斉反応の開発に取り組んでいます。
特に、ペプチドのLate-stageにおける立体制御に注目しています。最近私たちは、ペプチド上のデヒドロアラニンに対する不斉反応が高い選択性で進行し、不斉配位子の使い分けによって、側鎖の影響を受けることなく両方の立体を選択的に構築できることを明らかにしました。
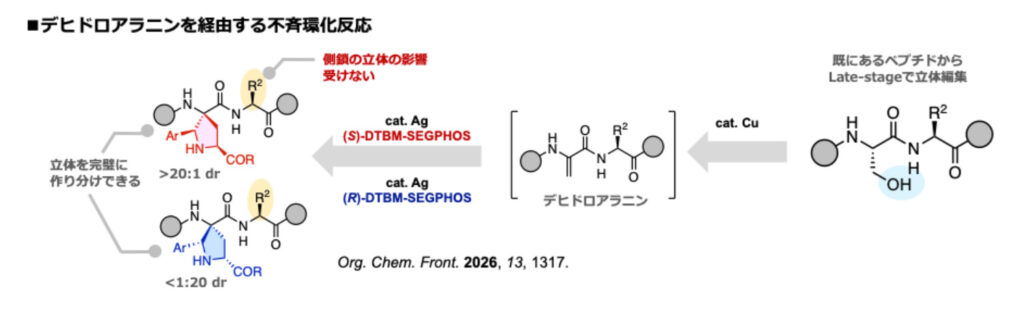
一方で、アミノ酸の不斉反応は豊富な知見が蓄積されているのに対し、ペプチドを対象とした不斉反応は未発展の領域です。そこで本研究では、アミノ酸化学で得られた知見を、計算科学を架け橋としてペプチド化学へと展開し、新たな不斉反応の開拓を目指します。また、現在はアミノ酸およびペプチド化学に資する不斉反応の開発を中心に進めていますが、これにとどまらず、多様な分子変換反応へと展開していきます。
<関連の業績>
ペプチド関連:
Org. Chem. Front. 2026, 13, 1317.
アミノ酸関連:
Org. Lett. 2024, 26, 1880.
Chem. Eur. J. 2023, 29, e202302609.
J. Org. Chem. 2023, 88, 924.
Chem. Asian J. 2022,17, e202200239.
J. Org. Chem. 2021, 86, 14586.
J. Org. Chem. 2020,85, 8142.
Eur. J. Org. Chem. 2019, 4561.
医薬品の工業生産にも利用できる実用的な試薬の開発
医薬品の開発において、活性の高い化合物を見出しても、安価で安定的な工業生産ができなければ、上市に漕ぎ着けることはできません。近年、医薬品構造の複雑化や新たなモダリティの出現により、大量生産の重要性が再認識されています。製薬企業での経験において、実際に、薬価との釣り合いが取れずにドロップアウトしていく候補化合物を数多く見てきました。このような観点から、有望な官能基を安価で簡便に導入できる「試薬」を開発することで、これらの官能基の創薬研究における地位を押し上げることが可能と考えています。
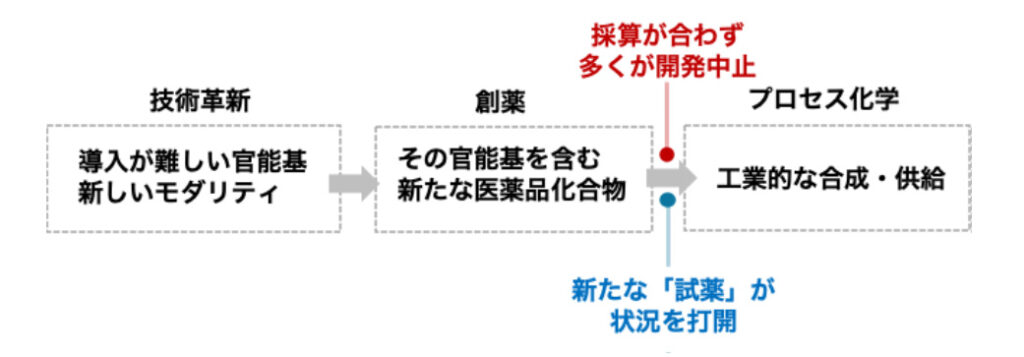
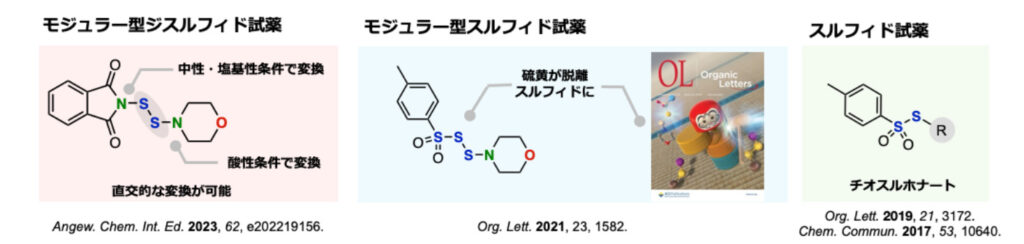
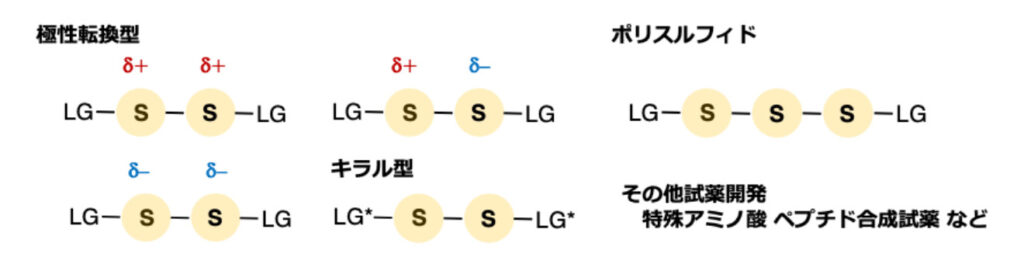
当研究室では、このような便利な試薬の開発を行うとともに、上記のようなジスルフィド化反応、ペプチド修飾反応を、スケールアップでも利用できるような堅牢な方法論に磨き上げることを目指します。これまでに、ジスルフィド試薬を始めとした有機硫黄試薬の開発に成功しており、ジスルフィド試薬は試薬メーカーでの発売を予定しています。このように多くの研究者が手に取って使いやすい状況を作ることで、その官能基の利便性が向上することを願っています。今後は硫黄試薬に限らないさらなる試薬レパートリーの充実を目指していきたいと考えています。将来的には、このような試薬や方法論が、実際の医薬品開発に利用されていくことを夢見ています。




